2026
La criopreservación embrionaria mediante procesos de vitrificación ha supuesto un avance en la medicina reproductiva, permitiendo optimizar los tratamientos de fertilidad y aumentar las tasas de gestación acumulada.
La transferencia de embriones congelados, también conocida como transferencia embrionaria en diferido, permite optimizar los tratamientos de fertilidad, ofreciendo la posibilidad de utilizar aquellos embriones de buena calidad que no se vayan a transferir en el ciclo inicial.
Este tipo de transferencia embrionaria exige previamente una exhaustiva preparación del endometrio materno y una sincronización milimétrica con el laboratorio de embriología, asegurando que el embrión desvitrificado encuentre el microambiente uterino idóneo para su correcta implantación.
1. Fases previas a la criotransferencia embrionaria
Antes de proceder a la transferencia del embrión a la cavidad uterina, es fundamental asegurar que el endometrio materno presente unas condiciones morfológicas y funcionales idóneas que favorezcan la implantación embrionaria. El éxito de la criotransferencia embrionaria depende en gran medida de esta sincronización biológica.
Para lograr este objetivo de sincronía celular, la medicina reproductiva establece un protocolo clínico minucioso dividido en distintas etapas evaluativas, con objeto de garantizar que el útero esté preparado antes de proceder a la descongelación (desvitrificación) embrionaria.
1.1.Preparación endometrial y grosor óptimo
La paciente recibirá medicación hormonal distinta a la de la estimulación ovárica para conseguir que su endometrio esté receptivo, es decir, sea capaz de interaccionar con el embrión para que éste implante dando comienzo al embarazo. En la mayoría de las ocasiones, la medicación para la preparación endometrial se realiza con estrógenos y progesterona administrados por vía oral, transdérmica en forma de parches o vaginal. Es posible también determinar el momento adecuado para la implantación embrionaria en un ciclo natural reduciendo al máximo la administración de medicación, si bien esto puede requerir controles adicionales y la normalidad del período menstrual.
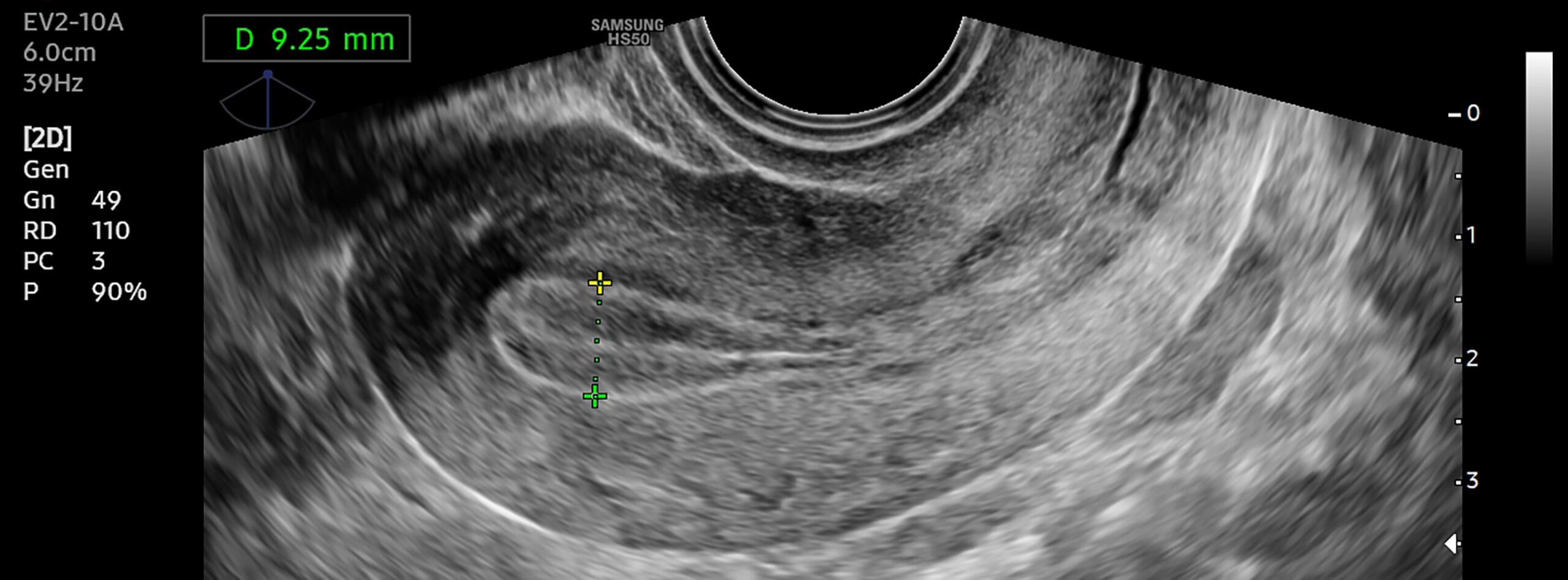
A nivel clínico, el monitoreo y control del endometrio se realiza mediante ecografías transvaginales seriadas. El seguimiento médico persigue lograr varios hitos anatómicos antes de autorizar el proceso de transferencia al útero materno:
- Conseguir un endometrio de aproximadamente un grosor de entre 7 y 10 mm y con aspecto trilaminar aproximadamente para favorecer la implantación embrionaria.
- Confirma que no existan irregularidades estructurales recientes en la cavidad uterina.
- En algunos casos, controlar los niveles séricos de hormonas para programar con exactitud el día óptimo en el que se transferirán los embriones previamente descongelados.
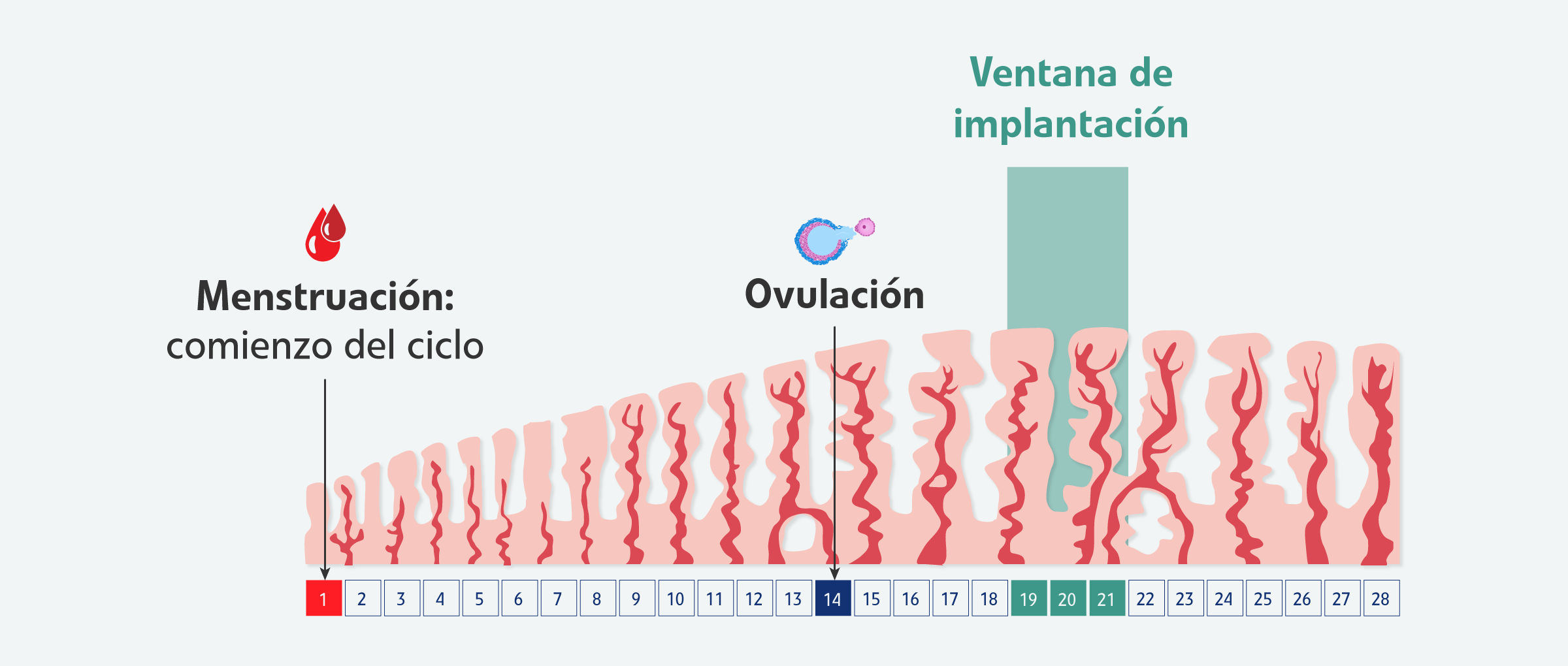
1.2.La ventana de implantación y receptividad
La receptividad uterina hace referencia a un estado concreto del endometrio en el que sus condiciones son óptimas para que suceda la implantación embrionaria. Cabe destacar que el endometrio solamente es receptivo unos determinados días del ciclo menstrual, exactamente entre 6-7 días tras la ovulación, periodo conocido biológicamente como la ventana de implantación.
En casos de fallos de implantación repetidos, se recurre a pruebas genómicas que estudian la receptividad del endometrio a nivel de los genes y su expresión molecular. Si existe un desajuste, se programará la transferencia embrionaria en otro momento del ciclo menstrual donde se demuestre que el endometrio está receptivo.
El estudio exhaustivo de esta fase incluye el análisis de múltiples variables biológicas a través de biopsias específicas:
- Expresión génica: pruebas moleculares que estudian la expresión de distintos genes asociados al estado receptivo del endometrio.
- Microbiota intrauterina: determinación de gérmenes patógenos y desequilibrios bacterianos mediante cultivos y técnicas de PCR.
- Despistaje de endometritis crónica: estudios anatomopatológicos utilizando la inmunohistoquímica con objeto de detectar estados inflamatorios del endometrio
- Evaluación inmunológica: control del ambiente de tolerancia inmunitaria local para evitar el rechazo embrionario materno.
2.Proceso de descongelación en el laboratorio
Una vez confirmada la idoneidad endometrial mediante ecografía y controles hormonales en sangre en algunos de los casos, el laboratorio de embriología procede a la desvitrificación embrionaria. Esta etapa requiere precisión técnica absoluta y control exhaustivo de los tiempos de exposición.
Se trata de un paso sumamente minucioso que involucra soluciones crioprotectoras inversas, devolviendo el embrión a su estado biológico funcional.
2.1.Tasa de supervivencia y técnica de desvitrificación
El procedimiento de desvitrificación embrionaria consiste en someter al embrión a un choque térmico inverso, extrayéndolo del nitrógeno líquido a -196ºC para sumergirlo en placas con medios de cultivo a 37ºC. Este ascenso de temperatura, combinado con soluciones de rehidratación progresiva, reactiva el metabolismo celular del embrión.
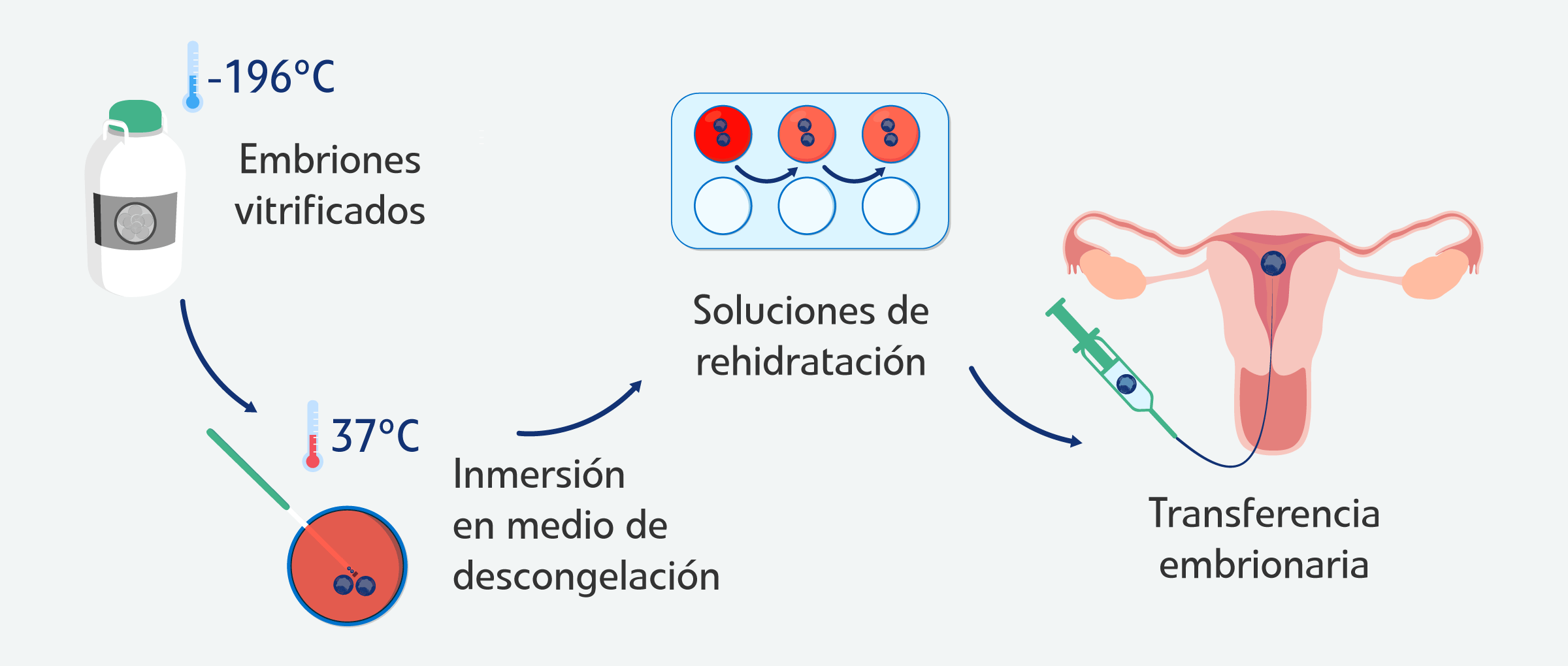
Gracias a los crioprotectores avanzados utilizados en la actualidad, las tasas de supervivencia embrionaria tras la desvitrificación son elevadas y la mayoría de los embriones superan este proceso.
3.El momento de la transferencia y la betaespera
Una vez desvitrificado el embrión, es el momento de transferirlo al útero de la paciente a través de una catéter específico. El personal de embriología es el encargado de cargar el embrión seleccionado en la cánula.
La transferencia embrionaria es indolora y de corta duración, tratándose de un proceso sencillo que se realiza sin necesidad de anestesia.
Una vez realizada la transferencia embrionaria, la paciente regresará a casa y podrá realizar su rutina diaria, aunque tratando de llevar una vida saludable evitando grandes esfuerzos. A partir de este momento comienza un periodo de incertidumbre para la paciente, la famosa betaespera. La mujer deberá esperar entre 10 y 12 días desde la transferencia embrionaria para hacer una prueba de embarazo y comprobar si la criotransferencia embrionaria ha tenido éxito.
4.Tasas de éxito y variables en la criotransferencia
Las estadísticas médicas internacionales reflejan que el uso de embriones criopreservados ofrecen probabilidades de gestación altamente consistentes y sumatorias. Esto desmonta el mito de que el frío reduce drásticamente las opciones reproductivas e incrementa la tasa acumulada final de embarazo. En muchos casos, optar por una transferencia embrionaria en diferido permite que el útero se recupere de la estimulación ovárica, ofreciendo un entorno más natural y receptivo.
Pese a ello, no hay que olvidar que la probabilidad de embarazo tras una transferencia en diferido, al igual que ocurre con la transferencia en fresco, dependerá de varios factores y no solo de si el embrión ha sido previamente congelado.
5. Preguntas frecuentes
- ¿Es dolorosa la transferencia de embriones congelados?
La transferencia embrionaria en diferido o de embriones vitrificados se cataloga como un procedimiento totalmente indoloro. Durante el procedimiento, las pacientes relatan percibir únicamente la molestia fisiológica leve provocada por la inserción del espéculo y la presión requerida, al necesitar en algunos casos mantener la vejiga parcialmente llena, sensaciones comparables a las de una revisión citológica rutinaria en la consulta ginecológica.
- ¿Cuánto tiempo máximo puede estar un embrión vitrificado?
El almacenamiento en tanques de nitrógeno líquido a -196 °C detiene por completo el metabolismo y la actividad de las células. A estas temperaturas extremas, no existe un deterioro biológico estructural provocado por el paso de los años, garantizando la viabilidad morfológica inalterada.
Por consiguiente, no existe una fecha de caducidad biológica. Los embriones pueden permanecer criopreservados durante décadas manteniendo idéntico potencial de implantación que el primer día de su congelación en el laboratorio.
- ¿Qué ocurre si el embrión no sobrevive a la descongelación?
Aunque la técnica de vitrificación actual ofrece tasas de supervivencia embrionaria superiores al 95%, existe un pequeño porcentaje de casos en los que el embrión no logra recuperar su viabilidad celular tras el proceso de calentamiento. Cuando esto sucede, el equipo de embriología constata que su desarrollo biológico se ha detenido o sus células han sufrido daños irreparables, por lo que deja de ser apto para ser transferido al útero materno.
Ante esta situación, el protocolo clínico a seguir dependerá directamente de la reserva embrionaria de la paciente. Si existen blastocistos o embriones adicionales criopreservados en el banco del laboratorio, los especialistas procederán a la descongelación de un nuevo embrión de la misma cohorte. Este procedimiento se realiza de forma ágil y permite, en la mayoría de las ocasiones, mantener la transferencia programada para ese mismo día sin alterar el ciclo de preparación endometrial.
Por el contrario, si no se dispone de más embriones congelados, será necesario cancelar la transferencia uterina. En este escenario, el equipo médico programará una nueva consulta para evaluar detenidamente el caso clínico y plantear las alternativas terapéuticas más pertinentes, como puede ser el inicio de un nuevo ciclo de estimulación ovárica para la obtención de nuevos ovocitos que generen más embriones.
- ¿Qué riesgos están asociados a la criotransferencia embrionaria?
El proceso clínico para la receptora en una transferencia embrionaria en diferido es altamente seguro y catalogado como mínimamente invasivo. Al no requerir una nueva estimulación ovárica ni una punción folicular, se suprime por completo el riesgo de padecer el síndrome de hiperestimulación ovárica (SHO) u otras complicaciones derivadas de la anestesia, por ejemplo.
El principal riesgo de la transferencia embrionaria en diferido a nivel biológico recae exclusivamente en el ámbito del laboratorio, ya que un pequeño porcentaje estadístico de embriones (habitualmente inferior al 5%) podría no sobrevivir adecuadamente al estrés osmótico de la desvitrificación celular, obligando a cancelar la transferencia embrionaria.

